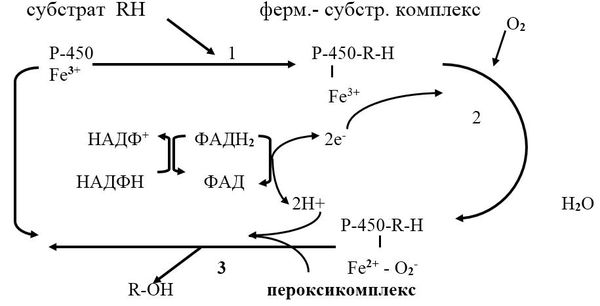
Рис. 11.1. Схема микросомального окисления
Микросомальное окисление протекает в несколько этапов:
1. связывание в активном центре цитохрома Р450 субстрата RН;
2. присоединение первого электрона и восстановление железа в геме до Fe; изменение валентности железа увеличивает сродство комплекса Р450 – Fe∙ RH к молекуле кислорода; присоединение второго электрона к молекуле кислорода и образование неустойчивого пероксикомплекса Р450–Fe∙ О2∙ RH;
3. Fe окисляется, при этом электрон присоединяется к молекуле кислорода; восстановленный атом кислорода (О2) связывает два протона (донор протонов – НАДФН+Н) и образуется 1 молекула воды; второй атом кислорода участвует в гидроксилировании субстрата RH; гидроксилированный субстрат ROH отделяется от фермента.
В результате гидроксилирования гидрофобный субстрат становится более полярным, повышается его растворимость и возможность выведения из организма с мочой. Так окисляются многие ксенобиотики, лекарственные вещества.
В редких случаях в результате гидроксилирования токсичность соединения увеличивается. Например, при окислении нетоксичного бензпирена (содержится в табачном дыму, копченостях) образуется токсичный оксибензпирен, который является сильным концерогеном, индуцирующим злокачественное перерождение клеток.
В митохондриях содержится монооксигеназная система, которая выполняет биосинтетическую функцию: синтез холестерола; стероидных гормонов (кора надпочечников, яичники, плацента, семенники); желчных кислот (печень); образование витамина D3 (почки).
Активные формы кислорода (свободные радикалы)
В организме в результате окислительно-восстановительных реакций постоянно происходит генерация активных форм кислорода (АФК) при одноэлектронном восстановлении кислорода (молекула имеет неспаренный электрон на молекулярной или внешней атомной орбите).
Источники АФК:
1. цепь тканевого дыхания (утечка электронов с восстановленного убихинона KoQH2 на кислород);
2. реакции, катализируемые оксидазами, гемопротеинами, цитохромом Р450;
3. реакции окисления в лейкоцитах, макрофагах и пероксисомах;
4. радиолиз воды;
5. под воздействием ксенобиотиков, пестицидов;
6. реакции самопроизвольного (неферментативного) окисления ряда веществ.
Супероксид-анион – является одним из наиболее широко распространенных в организме свободных радикалов:
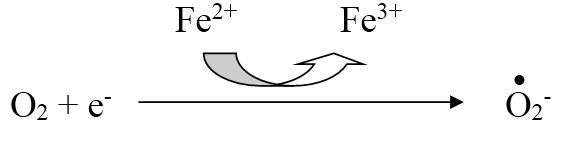
Он образуется в клетках болезнетворных бактерий и является повреждающим фактором для мембран клеток паренхиматозных органов человеческого организма. Для лейкоцитов и макрофагов супероксид-анион является фактором бактерицидности, с помощью которого клетки инактивируют патогенные микроорганизмы.
Другой путь образования свободных радикалов – взаимодействие кислорода с металлами переменной валентности. При этом образуется пероксидный радикал:
Fe + O2 + H → Fe + •HO2
•O2 + Н → •HO2
Взаимодействие супероксиданиона с пероксидным радикалом (1) или одноэлектронное восстановление супероксид-аниона (2) в водной среде приводят к образованию пероксида водорода
•O2 + •НО2 + Н → Н2О2 + О2 (1)
•О2 + е + 2Н → Н2О2 (2)
Гидроксильный радикал ОН образуется при взаимодействии пероксида водорода с супероксид-анионом (1) либо с металлами (2):
Н2О2 + •О2 → •ОН + ОН + О2 (1)
Н2О2 + Fe → •ОН + ОН + Fe (2)
Кислородные радикалы обладают высокой реакционной способностью и легко вступают в химические реакции с органическими молекулами для приобретения недостающего электрона. Кислородные радикалы оказывают воздействие на различные структурные компоненты клеток: ДНК (повреждение азотистых оснований); белки (окисление аминокислотных остатков, образование ковалентных "сшивок"); липиды; мембранные структуры.
Активные формы кислорода могут отщеплять электроны от многих соединений, превращая их в новые свободные радикалы, и инициируют тем самым цепные окислительные реакции. Если в реакцию с АФК вступают ненасыщенные жирные кислоты плазматических мембран, говорят о перекисном окислении липидов.
Перекисное окисление липидов (ПОЛ)
Реакции ПОЛ являются свободнорадикальными и постоянно протекают в организме, также как и реакции образования АФК.
В норме они поддерживаются на определенном уровне и выполняют ряд функций:
1. индуцируют апоптоз (запрограммированную гибель клеток);
2. регулируют структуру клеточных мембран и тем самым обеспечивают функционирование ионных каналов, рецепторов, ферментных систем;
3. обеспечивают освобождение из мембраны арахидоновой кислоты, из которой синтезируются биорегуляторы (простагландины, тромбоксаны, лейкотриены);
4. ПОЛ может выступать в качестве вторичного мессенджера, участвуя в трансформации сигналов из внешней и внутренней среды организма, обеспечивая их внутриклеточную передачу;
5. АФК участвуют в клеточном иммунитете и фагоцитозе.
Механизм ПОЛ:
1. Инициация. Инициирует реакцию чаще всего гидроксильный радикал, отнимающий водород от СН2- групп ненасыщенной жирной кислоты L, что приводит к образованию липидного радикала L•:
L + •OН → L•
2. Развитие цепи. Развитие цепи происходит при присоединении кислорода, в результате чего образуется пероксидный радикал LOO• или пероксид липида LOOH (гидроперекиси липидов)
L• + O2 → LOO•
LOО• + LH → LOOH + LR∙•
3. Обрыв цепи. Развитие цепи может останавливаться при взаимодействии свободных радикалов между собой или при взаимодействии с различными антиоксидантами (витамином Е), которые являются донорами электронов:
LOO•∙ + L• → LOOH + LH
L∙•+ Витамин Е → LH + Витамин Е•∙