Всего за 69.9 руб. Купить полную версию
Эффективность кишечного клиренса зависит от состояния мигрирующего моторного комплекса (ММК, англ. Migrating motor complex) – циклической, стереотипно повторяющейся сократительной активности желудка и тонкой кишки в межпищеварительный период. В норме сокращения и расслабления в двенадцатиперстной кишке происходят с периодичностью в среднем около 11 / мин, постепенно уменьшаясь к подвздошной кишке до 7 / мин. У здоровых людей регулярные сокращения с этой частотой продолжаются около 5 минут с промежутками от 20 мин до 1 часа (Husebye E., 1999; Vantrappen G., 1977). Общая продолжительность цикла мигрирующего моторного комплекса – около 90–120 минут. Сокращения, возникающие в рамках ММК, обеспечивают продвижение по тонкой кишке пищеварительных соков, остатков пищи, слизи, в том числе и бактерий.
Условиями для нормального кишечного клиренса являются сохраненная анатомическая целостность и функциональная активность кишечника (отсутствие хирургических вмешательств, врожденных аномалий, нормальная перистальтика и др.). Косвенным индикатором сохраненного кишечного клиренса является отсутствие в тонкой кишке грамотрицательной флоры. Снижение перистальтики тонкой кишки и / или изменение ее нормальной анатомии приводит в итоге к стазу содержимого, создает благоприятные условия для избыточного роста грамотрицательной флоры (Мечетина Т. А., 2011; Кучерявый Ю. А., 2010).
Хронические заболевания панкреато-билиарной системы, сопровождающиеся объемным снижением секреции желчи и панкреатического сока и приводящие как к несостоятельности дуоденального антибактериального барьера, так и к грубым нарушениям пищеварения в верхнем отделе пищеварительнотранспортного конвейера, в первую очередь жиров, являются триггером для избыточного роста микрофлоры в тонкой кишке (Кучерявый Ю. А., 2010).
Мечетина Т. А. (2011) указывает на потерю концентрационной функции желчного пузыря после холецистэктомии как на один из факторов, способствующих формированию СИБР в тонкой кишке. В физиологических условиях стерильность желчи обеспечивается антибактериальным эффектом желчных кислот (Малафеева Э. В., 1996). Бактерицидные свойства пузырной желчи по сравнению с печеночной, существенно выше, так как концентрация желчных кислот за счет его всасывательной функции увеличивается примерно в 10 раз. При нормально функционирующем желчном пузыре после еды желчь выбрасывается сразу большой порцией и транзиторная микрофлора, находящаяся в двенадцатиперстной кишке, в большинстве своем гибнет.
Желчные кислоты расщепляют эндотоксины, выделяемые грамотрицательной флорой тонкой кишки на нетоксичные фрагменты (Bertok L., 2004), а также воздействуют непосредственно на клеточные мембраны бактерий. Периоды заполнения и опорожнения желчного пузыря имеются в течение каждой из фаз ММК, однако максимум выделения желчи наблюдается, когда сокращения третьей фазы (максимальной активности) ММК достигают подвздошной кишки. Снижение бактерицидных свойств желчи неминуемо создает благоприятные условия для развития СИБР в тонкой кишке.
Антибактериальной активностью обладает и панкреатический сок, являющийся одним из важных компонентов врожденной защиты желудочно-кишечного тракта (Rubinstein E., 1985; Kruszewska D., 2004; Holowachuk S. A.,2004;. Minelli E. B., 1996)
Противоречивые данные в литературе приведены относительно патогенетической связи СИБР и хронических воспалительных заболеваний кишечника. Развитие хронических заболеваний кишечника рассматривается с позиций гипотезы о существовании микроботканевого комплекса кишечника – функционального блока, объединяющего эти три составляющие (Денисов Н. Л., 1997). Местной иммунной системе отводится основная регуляторная роль в обеспечении равновесного состояния в микроботканевом комплексе (Денисов Н. Л., 1990). При этом отмечается единство структуры слизистой оболочки и локальной иммунной защиты желудочно-кишечного тракта (Brandtzaeg P., 1995). В целом эффективная защита определяется сбалансированным ответом всех звеньев местного иммунитета, однако ведущим фактором, по мнению всех исследователей, является sIgA (Tsuji M., 2008; Wines B. D., 2006).
Недостаточность этого компонента влечет за собой колонизацию слизистых оболочек микробами (Nagura H., 1998), повышение потока аллергенов через эпителиальный барьер (Macdonald T. T., 2005) и, как следствие, повышение нагрузки на "вторую линию" иммунной защиты, с формированием хронического воспаления (Powrie F., 2004).
Многие авторы отмечают наличие СИБР и его участие в патогенезе при синдроме раздраженного кишечника (Leung Ki E. L., 2010; Lin H. C., 2005). Так, СИБР был найден приблизительно в 25 % пациентов страдающих болезнью Крона, особенно у больных переносших операцию (Castiglione F., 2003). Однако, Денисов Н. Л. (2011) в своей работе определил некоторую тенденцию взаимоотношения хронических воспалительных заболеваний (ХВЗ) кишечника и СРК. Так при анализе тонкокишечных аспиратов у пациентов с СРК выявлялось достоверно большее микробное число, чем у здоровых лиц, но меньшее, чем у больных язвенным колитом (1,47; 1,3 и 4,88 lg КОЕ / мл соответственно). Усиление пролиферации условно-патогенной микрофлоры происходило на фоне выраженной депрессии основных представителей нормального микробиоценоза кишечника и наблюдалось преимущественно у больных язвенным колитом.
Описанная тенденциозность "выстраивает" состояние здоровья, функциональную патологию кишечника и ХВЗ кишечника в линейный график развития воспаления. Иными словами, функциональная патология кишечника в условиях СИБР проявляется менее выраженными воспалительными проявлениями в стенке кишки, чем хронические воспалительные заболевания кишечника, что неоднократно доказано гистологически, инструментально и клинически, и однозначно отвечает на вопрос от неправомерности применения термина "функциональное заболевание кишечника". Очередным подтверждением сказанного является двух– трехкратное превышение нормы белка кальпротектина в фекалиях пациентов с недостаточностью баугиниевой заслонки. По нашим данным у 97 % (n=26) обследованных пациентов с доказанной по результатам ирригоскопии НБЗ кальпротектин составил в среднем 162,4 мкг / г, при норме 0–49 мкг / г.
Клиника СИБР. Мечетина Т. А. (2011) указывает на то, что клинические проявления СИБР в тонкой кишке обусловлены характером патологических процессов, развивающихся вследствие различных причин, и носят вторичный характер.
Плотникова Е. Ю. 2013 определяя симптомы СИБР (метеоризм, вздутие живота, абдоминальная боль или дискомфорт, диарея, утомляемость, слабость, похудание), отмечает что, они не характеризуются специфичностью, а отражают степень распространенности воспаления слизистой оболочки кишки, "наслаиваются" на проявления основного заболевания, являющегося причиной развития СИБР. Более тяжелые симптомы, включая мальабсорбцию (потеря веса, стеаторея, мальнутриция), дефицит нутриентов (анемия, тетания при гипокальциемии индуциорованной дефицитом витамина Д, В 12 – дефицитная полиневропатия) и расстройство метаболизма костной ткани, повреждение печени указывают на осложнения СИБР (Saltzman J. R., 1994; Кучерявый Ю. А., 2010).
Клиническая картина СИБР неспецифична и полиморфна и позволяет только предполагать клинический диагноз. Можно выделить ряд наиболее часто встречаемых симптомов, которые условно можно разделить на абдоминальные (объективный метеоризм, особенно через небольшой промежуток после приема пищи, неустойчивый стул со склонностью к диарее, лиентерея и стеаторея) и общие (признаки дефицита жирорастворимых витаминов, цианокобаламина и фолиевой кислоты, железа; невротические расстройства) (Кучерявый Ю. А., 2010).
Патоморфоз синдрома избыточного бактериального роста нередко маскируется под соматические заболевания и во многом напоминает мальабсорбцию при СРК с диареей (Donaldson R. M. Jr., 1964; King T., 2004; Lin H. C., 2004; Saltzman J. R., 1994; Lupascu A., 2005). Метеоризм, абдоминальный дискомфорт и боли, расстройства стула в сторону послабления – вот немногое из того, что роднит эти два состояния, и то, о чем весьма часто сообщают сами пациенты (Кучерявый Ю. А., 2014). Если учесть, что в ряде случаев СИБР протекает вообще бессимптомно (Маев И. В., 2011; Bures J., 2010; Gabrielli M., 2013), а бактерии довольно значительно влияют на ферментативные, метаболические процессы и сорбцию, то рано или поздно могут появиться признаки мальабсорбции и альдигестии, напоминающие симптоматику СРК, за исключением постоянности связи боли и метеоризма со стулом.
Ассоциация СИБР и СРК способствует формированию синдрома мальабсорбции за счет сочетания двух важнейших факторов: ускоренный пассаж (уменьшение времени контакта химуса с эпителиоцитами тонкой кишки) и избыточная активность бактерий в тонкой кишке с инактивацией панкреатических ферментов (вторичная панкреатическая недостаточность). Нарушение моторной функции кишечника у больных с СРК может служить фоном или фактором риска развития / прогрессирования СИБР. Роль кишечной микрофлоры для организма человека очевидна: когда в силу разных причин она занимает новую экологическую нишу или число микроорганизмов в естественном биотопе превышает условно определенный нормальный барьер, могут появиться клинические симптомы, функциональные расстройства и, возможно, повышаться риск органических изменений различных органов, вплоть до развития осложнений.
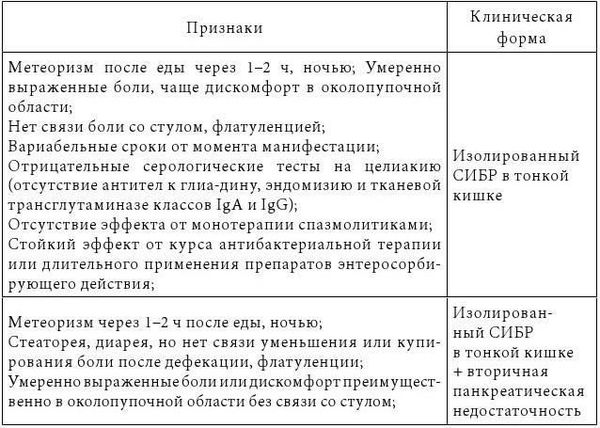
Кучерявый Ю. А. (2014) выделил возможные сочетания СИБР и СРК и дал их клиническую характеристику (табл. 3).
Таблица 3
Клинические сочетания СИБР и синдрома раздраженного кишечника